
曾于2015年处方药销售金额达232.64亿美元而以排名第9位挺进全球制药Top10榜单的阿斯利康于2016年以多起业务出售交易频频登上医药行业的头条。阿斯利康在神经、呼吸、消化、心血管/代谢、肿瘤和麻醉等领域有多个产品一直处于全球领先地位,特别是全球首个获批上市的洛赛克堪称是创下了医药行业的传奇。不过,让大多数精神分裂症患者重返社会的思瑞康给大多数曾伤心欲绝的家庭带来了新希望。然而,近年来阿斯利康因多个产品遭遇专利悬崖而使其销售额大幅度下滑,我们难免会问阿斯利康未来都有哪些拳头产品,洛赛克时代是否会昔日重来等等。好啦,雷诺现在带领大家穿越时空一起去看看未来阿斯利康都有哪些产品。
来自EvaluatePharma数据显示,2022年阿斯利康Top 10的产品全球销售额均逾10亿美元以上。在这Top 10的产品中,有8个小分子类药物,2个生物类药物。值得一提的是,这2个生物类药物目前尚处于III期临床试验阶段,而其余8个小分子药物均已在美国上市(详见表1)。
好了,让我们先睹为快,先来看看Top 5产品的未来市场走势(详见图1)。
表1 2022年阿斯利康Top 10的产品
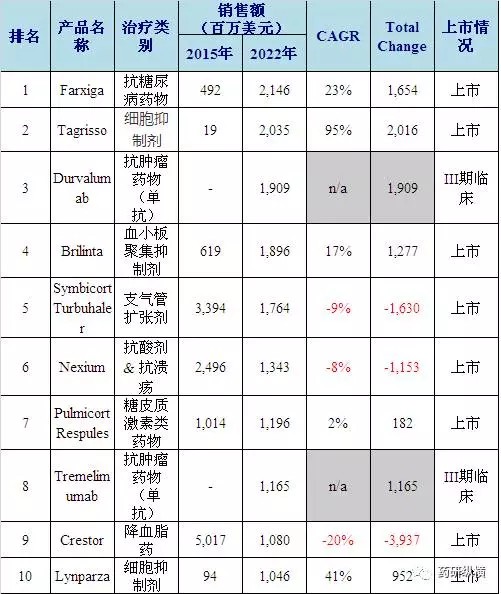
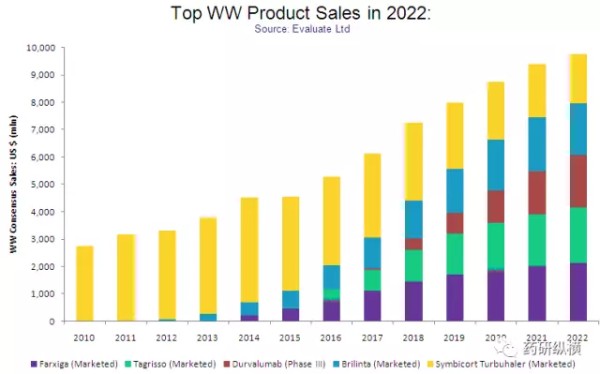
图1 2022年阿斯利康Top5产品走势
Top 1:Farxiga(Dapaglifozin)
于2014年获美国FDA批准的Farxiga是一种钠-葡萄糖协同转运蛋白2(SGLT2)抑制剂,用于治疗成人II型糖尿病。Farxiga是美国FDA继Invokana之后批准的第2款SGLT2药物。Farxiga的有效性和安全性较好,其对SGLT2的选择性比对SGLT1的选择性高1000~3000倍。Farxiga可降低对其它器官的副作用,改善体内糖化血红蛋白HbA1c的含量,降低了低血糖的发生。Farxiga 还有轻度的利尿作用,更适合患有高血压的II型糖尿病患者。
Farxiga上市剂型为片剂,规格有5mg和10mg。美国FDA橘皮书显示,其在美国的核心专利有US6515117(到期时间:2020-10-04),US85101698(到期时间:2027-06-20),US8361972(到期时间2028-03-21),以及US8685934(到期时间:2030-05-26)等。
2022年,Farxiga的全球销售额将达21.46亿美元,有望成为抗糖尿病药物的佼佼者。
本品目前尚未在中国上市。
Top 2:Tagrisso(Osimertinib)
于2015年11月13日获美国FDA批准的Tagrisso属第三代酪氨酸激酶抑制剂(TKI)类靶向药物。Tagrisso是一种片剂,规格有40mg和80mg。Tagrisso是美国FDA批准的首个用于经EGFR-TKI治疗时或治疗后病情进展的T790M突变阳性非小细胞肺癌(NSCLC)的药物,可满足T790M耐药突变患者人群的临床需求。Tagrisso的问世为T790M耐药突变的治疗提供了新的治疗方案,具有划时代里程碑式意义。
Tagrisso具有口服生物利用度高,副作用小的特点。其临床优势表现在可延长EGFR突变患者的无复发存活期,且对心脏和血糖的影响甚微。此外,早期的临床研究证实,Tagrisso对NSCLC脑转移患者有效。
美国FDA橘皮书显示其在美国的核心专利有US8946235(到期时间:2032-08-08)。
2022年,Tagrisso的全球销售额有望突破20亿美元。
本品目前尚未在中国上市。
Top 3:Durvalumab
雷诺曾在《全球估值最高的TOP 10在研药物》一文中有简单介绍过Durvalumab,因此本文将不再对Durvalumab做过多介绍。近年来,有关PD-1/PD-L1免疫疗法的报道层出不穷。尽管阿斯利康的Durvalumab已落后百时美-施贵宝、默克和罗氏许多,但阿斯利康对Durvalumab仍信心满满。不过,谁将成为下一个赢家我们拭目以待。
Top 4:Brilinta(Ticagrelor)
于2011年7月获美国FDA批准的Brilinta是一种环戊三唑嘧啶类化合物,用于减少急性冠脉综合征(ACS)患者的心血管死亡和心脏病发作。Brilinta及其代谢物能可逆性地与血小板P2YADP受体相互作用,阻断信号传导和血小板活化。Brilinta具有起效迅速,能有效改善急性冠心病患者临床症状的特点。Brilinta适用于那些需在先期进行抗凝治疗后再行手术的患者。 与波立维相比,Brilinta还具有抗血小板作用更强,更持久的特点。目前,Brilinta已被多部国际治疗指南推荐用于ACS患者的一线治疗,其临床地位已越发凸显。
Brilinta是一种片剂,规格有60mg和90mg。美国FDA橘皮书显示其在美国的核心专利有US7250419(到期时间:2019-12-02),US7265124(到期时间:2021-07-09),US6251910(到期时间:2018-07-15)和US8425934(到期时间:2030-04-17)等。
本品已进口中国,且已被《急性冠脉综合征急诊快速诊疗指南》所推荐。
预计2022年,Brilinta的全球销售额为18.96亿美元。
Top 5:Symbicort Turbuhaler
Symbicort Turbuhaler是一种用于治疗哮喘的吸入糖皮质激素布地奈德和吸入长效β2受体激动剂福莫特罗的新型复方干粉吸入剂。Symbicort Turbuhaler通过不同的作用机理在减轻哮喘的加重方面有协同作用。其中,布地奈德对肺具有糖皮质激素的抗炎作用,可减轻哮喘症状,阻缓病情恶化,且相对副作用比全身性用药少。福莫特罗对有可逆性气道阻塞的患者有舒张支气管平滑肌的作用。临床试验证实,与舒利迭相比,Symbicort Turbuhaler可降低慢性肺阻塞性疾病急性加重风险,以及降低肺炎风险(73%)和因肺炎导致的住院风险(74%),显著减少肺炎相关死亡风险(76%)。
美国FDA橘皮书显示,Symbicort Turbuhaler在美国的核心专利有US7759328(到期时间:2023-01-29),US7367333(到期时间:2018-11-11),US7967011(到期时间:2021-08-11),US8616196(到期时间:2029-04-07)等。
因价格压力和欧美等市场需求逐渐降低,Symbicort Turbuhaler近年来的销售额也呈下滑趋势。预计2022年,Symbicort Turbuhaler的全球销售额将跌至17.64亿美元。
本品已进口中国,目前其在中国的销售额仍呈上升趋势。据悉,2015年国内样本医院销售额为2.35亿元,同比增长21.8%。
Top 6:Nexium
有关Nexium方面的信息实在太多,相信大家已不再陌生啦。“五色令人目盲;五音令人耳聋”,雷诺在此就不对Nexium做过多介绍。弹指间,Nexium已在美国问世近16年。Nexium也因此成为继洛赛克之后全球最畅销的质子泵抑制剂。Nexium曾于2008年创下全球销售额50亿美元的佳绩,不过遭遇专利悬崖即将与通用名药物相竞争的Nexium未来市场走势究竟又会怎样呢?图2是最好的诠释。预计2022年Nexium全球销售额仅13.43亿美元,可见昔日繁华将不再。尽管本品国内关注度非常之高,仿制的药企一浪高过一浪,但迄今为止,国内仅重庆莱美药业一家企业获生产批文。毋庸置疑,首仿成功的莱美药业获得了准入国内市场的第一张通行证,但莱美药业目前尚未对Nexium的国内市场造成实质性威胁。不过,未来景象如何期待着吧!
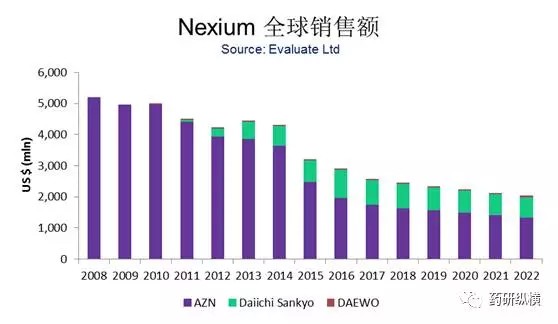
图2 Nexium全球销售额及未来销售预期
Top 7:Pulmicort Respules
于2000年8月8日获美国FDA批准上市的Pulmicort Respules是一种吸入用布地奈德混悬液,临床上用于治疗支气管哮喘。临床试验证实,Pulmicort Respules能有效地控制急性喘息、咳嗽和呼吸困难等症状,可减少全身副作用,且安全性良好。Pulmicort Respules适用患者人群比较广,包括儿童在内。
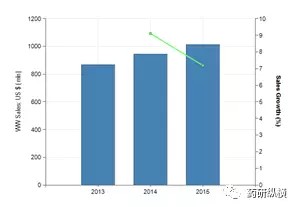
图3 2013-2015年Pulmicort Respules全球市场态势
近3年来,Pulmicort Respules全球销售额仍呈增加趋势(详见图3)。2015年全球销售额为10.14亿美元,同比增长7%。预计2022年,Pulmicort Respules的全球销售额为11.96亿美元。
据悉,2015年国内样本医院销售额为5.97亿元,同比增长13.3%。国内未来市场走势预计还会呈增长趋势。
Pulmicort Respules的专利将于2019年6月到期。
Top 8:Tremelimumab
Tremelimumab是一种阻滞CTLA-4与配体结合的人 IgG2 单克隆抗体,通过结合表达于活化的T淋巴细胞表面的CTLA-4蛋白,刺激机体免疫系统对肿瘤细胞发起攻击。目前Tremelimumab正处于III期临床试验阶段。一项在87例局部晚期或转移性NSCLC患者中参与的II期临床研究结果显示,Tremelimumab治疗的有效率(RR)为4. 8%,与最佳支持治疗组比较,PFS并无显著改善。Tremelimumab曾于2015年被FDA授予恶性间皮质瘤治疗孤儿药地位。然而,在有571例患者参与的用于治疗间皮瘤的II期临床试验中,Tremelimumab作为二三线药物并未达到改善OS这一主要终点。
尽管EvaluatePharma预计2022年Tremelimumab的全球销售额有望达11.65亿美元,但其未来“钱”景如何,仍颇有点担忧。
Top9:Crestor()
于2003年8月获美国FDA批准的Crestor是继立普妥之后的另一个重磅炸弹级降血脂药物。Crestor是一种片剂,规格有5,10,20和40mg。2013年Crestor的销售额达60亿美元。不过,近年来Crestor的销售额逐年呈下滑趋势,2015年仅50.17亿美元。Crestor已于2016年5月专利到期。据悉,美国FDA现已批准Apotex、Mylan、TEVA和Watson等企业的Crestor版的通用名药物上市。随着多家仿制药公司通用名药物的市场涌入,Crestor给阿斯利康带来的业绩压力不言而喻。预计2022年,Crestor的销售额仅10.80亿美元。
本品已于2007年4月以商品名“可定”进口中国。可定在中国上市后市场表现不俗。据悉,2015年可定的样本医院销售额5.54亿元,同比增长36%。不过,随着鲁南贝特、浙江京新、南京正大天晴、南京先声东元、浙江海正和海南通用三洋等本土企业通用名药物的上市以及临床应用,预计将对可定冲击不小。
Top 10:Lynparza(Olaparib)
于2014年12月19日获美国FDA批准的Lynparza是一种50mg的片剂,临床上用于治疗BRCA1/2基因缺陷相关的晚期卵巢癌。Lynparza是一种多聚二磷酸腺苷核糖聚合酶(PARP)抑制剂。除对卵巢癌效果明显外,Lynparza还对三阴性乳腺癌,黑色素瘤,胃癌,胰腺癌,大肠癌和前列腺癌等有一定的效果。值得一提的是,在一项名为TOPARP-A的II期临床试验研究结果显示,Lynparza可阻止前列腺癌生长,减少血液中循环肿瘤细胞计数。Lynparza也因此于2016年1月获美国 FDA 授予突破性疗法资格,在既往接受过一种基于紫杉烷的化疗及至少一种最新激素药物治疗的患者中,用于BRCA1/2 或 ATM 基因突变转移性去势抵抗性前列腺癌 (mCRPC) 治疗。
预计2022年,Lynparza的全球销售额有望突破10亿美元。
本品目前正在中国进行临床试验。
作者:雷诺岛,邮箱:[email protected],公众号:药事纵横(pharmaguider),请文明转载,转载请注明来源和作者,否则一律视为侵权,侵权必究返回搜狐,查看更多
责任编辑:

